
Περιεχόμενο
Τα ισομερή αποτελούνται από ίδιους τύπους αλλά διαφορετικές δομές ή χωροταξικές ρυθμίσεις. Εμφανίζονται στη φύση, αλλά προκαλούν ένα ιδιαίτερο ενδιαφέρον για την οργανική χημεία - τη μελέτη των ενώσεων άνθρακα - λόγω της μεγάλης ποικιλίας οικονομικά σημαντικών οργανικών μορίων. Οι επιστήμονες προσπαθούσαν να αντλήσουν μαθηματικά τον αριθμό των ισομερών των οργανικών μορίων γραμμικής αλυσίδας, που ονομάζονται αλκάνια, αλλά δεν βρήκαν απλή σχέση μεταξύ του αριθμού των ισομερών και της ποσότητας του άνθρακα. Ωστόσο, τα υπολογιστικά προγράμματα που αποσυνθέτουν τις αλκάνες σε θραύσματα είναι ευκολότερο να λειτουργούν με καλά αποτελέσματα.
Τύποι ισομερών
Οι δύο τύποι ισομερών είναι δομικά και οπτικά. Τα δομικά ισομερή έχουν διαφορετικές διατάξεις ατόμων ή μικρών συστάδων ατόμων, που ονομάζονται λειτουργικές ομάδες. Αυτά τα ισομερή προκύπτουν από τις διαφορές στις διακλαδώσεις των μορίων και την οργάνωση των λειτουργικών ομάδων. Τα οπτικά ισομερή ή τα στερεοϊσομερή είναι δομικά πανομοιότυπα αλλά διαφέρουν στη χωρική γεωμετρική θέση των ατόμων και των λειτουργικών ομάδων. Παραδείγματα οπτικών ισομερών περιλαμβάνουν εικόνες καθρέφτη και μόρια που περιστρέφονται σε αντίθετες κατευθύνσεις.
Γνωρίστε τα αλκάνια
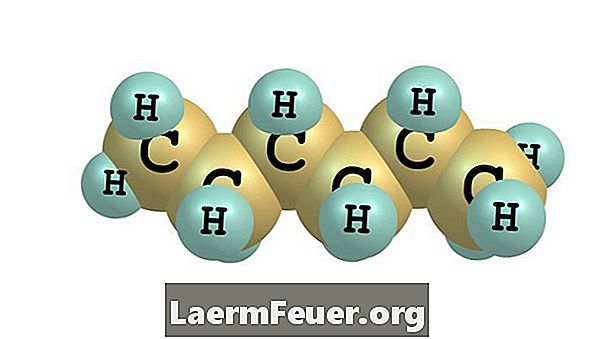
Τα αλκάνια είναι αλυσίδες ατόμων άνθρακα (C) και υδρογόνου (H), διατεταγμένα έτσι ώστε για κάθε n άτομα άνθρακα να υπάρχουν 2n + 2 υδρογόνα. Προέρχονται κυρίως από φυσικό αέριο και αργό πετρέλαιο. Ο άνθρακας στα αλκάνια σχηματίζει αλυσίδες στις οποίες κάθε άνθρακας δεσμεύεται σε τέσσερα άλλα άτομα με δεσμούς C-C ή C-H. Τα γραμμικά ή ακυκλικά αλκάνια δεν σχηματίζουν δακτυλίους. Το απλούστερο αλκάνιο είναι το μεθάνιο, το CH4. Αυτοί με τέσσερα ή περισσότερα άτομα άνθρακα μπορούν να σχηματίσουν δομικά ισομερή και αυτά με επτά ή περισσότερους άνθρακες μπορούν επίσης να σχηματίσουν οπτικά ισομερή. Μερικά ισομερή είναι "στερικά δυσμενή", πράγμα που σημαίνει ότι ο σχηματισμός τους είναι απίθανος επειδή χρειάζονται πολλή ενέργεια για να παραμείνουν σταθερά.
Μετρώντας τα ισομερή
Ο Robert Paton και ο Jonathan Goodman του Πανεπιστημίου του Cambridge προσφέρουν μια δωρεάν εφαρμογή που ονομάζεται IsoCount, η οποία υπολογίζει τον αριθμό των δομικών και οπτικών ισομερών οποιουδήποτε ακυκλικού αλκανίου. Απλά πληκτρολογείτε τον αριθμό των αλκανίων και το πρόγραμμα αποκαλύπτει τον αριθμό των δομικών και οπτικών ισομερών, λέγοντάς σας πόσοι είναι στερικά δυσμενείς. Το πρόγραμμα χρησιμοποιεί έναν αλγόριθμο που εξετάζει διαδραστικά το τμήμα του αλκανίου για να αντλήσει την ποσότητα των ισομερών. Για παράδειγμα, εάν εισαγάγετε επτά, το πρόγραμμα αναφέρει ότι το C7H16 αλκάνιο έχει εννέα δομικά και δύο οπτικά ισομερή.
Ασταθείς αλκάνες
Τα αλκάνια που έχουν 16 και 17 άνθρακες δεν είναι σταθερές ενώσεις και θα διαχωρίζονται γρήγορα σε θερμοκρασία δωματίου. Το C17 δεν υπάρχει και το C16 μπορεί να σχηματιστεί μόνο γρήγορα σε πολύ χαμηλές θερμοκρασίες. Ορισμένα αλκάνια μεγαλύτερων αλυσίδων είναι επίσης ασταθή. Το πρόγραμμα IsoCount θεωρεί τα θραύσματα άνθρακα ασταθή όταν αναφέρουν τα αποτελέσματά τους. Ο αριθμός ισομερών αυξάνεται ταχέως με τον αριθμό των ανθράκων. Οι συντάκτες του IsoCount εκτιμούν ότι τα ισομερή ενός αλκανίου 167-άνθρακα θα ξεπεράσουν τον αριθμό των σωματιδίων στο σύμπαν.